
2.2.7 РыШЅЛљЭХЕФаЇгІ
дкДѓЖрЪ§ЗМЯуЧзЕчШЁДњЗДгІРяЃЌРыШЅЛљЭХЪЧHЃЋЃЌЙигкЦфЫќРыШЅЛљЭХЕФЯрЖдЕФelectrofugalФмСІЃЌЫљзіЙЄзїВЛЪЧКмЖрЁЃПЩЪЧЃЌШЯЮЊРыШЅЛљЭХЕФФмСІЪЧЯТУцЕФЫГађЃКЃЈ1ЃЉЖдРыШЅВЛгУажњЕФРыШЅЛљЭХЃЈЯрЖдгкРыШЅЛљЭХЕФSN1Й§ГЬЃЉЃК
NO2ЃЋ<iЃPrЃЋЁЋSO3<t-Bu+ЁЋArN2+<ArCHOH+<NO+<CO2ЃЛЃЈ2ЃЉЖдРыШЅашгЩЭтУцЧзКЫЪдМСажњЕФРыШЅЛљЭХЃЈSN2Й§ГЬЃЉЃКMeЃЋ<ClЃЋ<BrЃЋ<D+ЁЋRCO+<HЃЋЁЋI+<Me3Si+ЁЃетжжЫГађПЩвдЫЕУїШЫУЧЙРМЦаЮГЩЪВУДбљЕФЗМЬўе§РызгЃЌДгЖјЕУЕНПЩФмЗЂЩњФФвЛИіЧзЕчШЁДњЕФИХФюЁЃЕЋЪЧЧБдкЕФРыШЅЛљЭХвВФмгАЯьдЪМЧзЕчЪдМСжБНгНјЙЅФЧИіЮЛжУЕФЫйЖШЁЃдкБЛЧтдзгвдЭтЕФЛљЭХШЁДњСЫЕФЮЛжУЩЯЕФЧзЕчНјЙЅЕФЗжЫйЖШвђзгНазіЃКЁАздЩэЫљдкЮЛжУЕФЗжЫйЖШвђзгЁБЃЈipso partial rate factorsЃЉЁЃ
3 ЧзКЫШЁДњЗДгІ
3.1 ЗДгІЛњРэ
ЗМЯузхЧзКЫШЁДњЗДгІЕФЛњРэжївЊгаЫФжжЁЃЦфжабаОПНЯЖрЕФЮЊЕЅЗжзгРњГЬЃЈSNAr1ЃЉЁЂЫЋЗжзгРњГЬЃЈSNAr2ЃЉКЭБНШВРњГЬЁЃСэЭтЃЌЕЅЗжзгИКРызгЛљРњГЬЃЈSRN1ЃЉвВдјМћжюБЈЕМЁЃ
3.1.1 SNAr1РњГЬ
SNAr1РњГЬдкЗМЯузхЧзКЫШЁДњЗДгІжаБШНЯЩйМћЁЃЪТЪЕЩЯЃЌжЛгазюгааЇЕФРыШЅЛљЭХЃЌШчжиЕЊЛљЭХЃЌВХАДетбљЕФРњГЬНјааЗДгІЃК
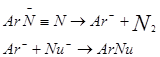
SNAr1РњГЬПЩвдЭЈЙ§вдЯТЪТЪЕжЄУїЃК
ЃЈ1ЃЉЗДгІЫйЖШдкжиЕЊбЮЮЊвЛМЖЃЌЖјКЭNuЃЕФХЈЖШЮоЙиЃЛ
ЃЈ2ЃЉМгШыИпХЈЖШЕФТБЫиИКРызгЃЌдђаЮГЩЕФВњЦЗЮЊТБДњЗМЯуЬўЃЌЕЋЗДгІЫйЖШгыМгШыЕФбЮЕФХЈЖШЮоЙиЃЛ
ЃЈ3ЃЉгЩБНЛљжиЕЊбЮаЮГЩБНЗгЕФЫйЖШЃЌдкЫЎжаКЭдкжиЫЎжавЛбљЃЛ
ЃЈ4ЃЉЗМЯуЛЗЩЯЕФЮќЕчзгШЁДњЛљНЕЕЭЗДгІЫйЖШЃЛЖјИјЕчзгШЁДњЛљЃЌдкМфЮЛЩЯЬсИпЗДгІЫйЖШЃЌдкЖдЮЛЩЯНЕЕЭЗДгІЫйЖШЃЛ
ЃЈ5ЃЉЪЙгУСкЮЛжиЧтЛЏЕФзїгУЮяНјааЗДгІЪБЃЌЭЌЮЛЫиаЇгІдМЮЊ1.22ЃЛ
ЃЈ6ЃЉРћгУБъМЧЕФбЧЯѕЫсКЭБНАЗЛђМзБНАЗзїгУЪБаЮГЩЕФжиЕЊбЮЃЌПЩвджЄУїЗДгІЕФЕквЛВНЪЧПЩФцЕФМќЖЯСбЃЛ
ЃЈ7ЃЉдкжиЕЊбЮЕФЗжНтзїгУРяаЮГЩЕФЬМе§РызгвВПЩЭЈЙ§ЧтзЊвЦЗДгІЕУЕНжЄУїЁЃ
3.1.2 SNAr2РњГЬ
ДѓВПЗжЗЂЩњдкЗМЯуЛЗЩЯЕФЧзКЫШЁДњЗДгІЖМАДSNAr2РњГЬНјааЁЃИУРњГЬАќРЈСНВНЃК
ЕквЛВНЃК
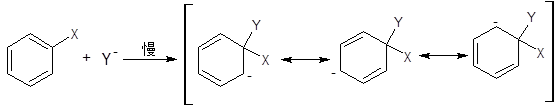
ЕкЖўВНЃК
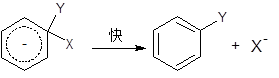
ЕквЛВНЭЈГЃЪЧОіЖЈЫйТЪЕФЃЌЕЋвВЪЧВЛвЛЖЈЁЃ
жЇГжИУРњГЬЕФжЄОнКмЖрЃЌШчЃКЗДгІЖЏСІбЇЁЂШЁДњЛљЁЂНщжЪаЇгІЃЌгШЦфЪЧЗДгІжаМфЬхЕФРыЮіКЭМјЖЈЁЃЯжМђвЊНщЩмШчЯТЃК
ЃЈ1ЃЉЖЏСІбЇ баОПНсЙћБэУїИУЗДгІЮЊЖўМЖЗДгІЃЛ
ЃЈ2ЃЉШЁДњЛљаЇгІ ДггаЙиЪЕбщзЪСЯПЩжЊЃЌЗМЯуЛЗЩЯЕФШЁДњЛљЖдЗДгІЫйЖШЕФгАЯьЪЧУїЯдЕФЃЛ
ЃЈ3ЃЉРыШЅЛљЭХ РыШЅЛљЭХЖдЗДгІЕФгАЯьвВБэУїЗДгІЪЧАДSNAr2РњГЬНјааЕФЃЛ
ЃЈ4ЃЉШмМСаЇгІ ЭЌбљжЄУїСЫЗДгІАДSNAr2РњГЬНјааЃЛ
ЃЈ5ЃЉМюЕФДпЛЏзїгУ ЭЌбљжЄУїСЫЗДгІАДSNAr2РњГЬНјааЃЛ
ЃЈ6ЃЉжаМфЬхЕФРыЮі ЗМЯузхЧзКЫШЁДњЗДгІЕФжаМфЬхЪБГЃОпгаЯрЕБЕФЮШЖЈадЃЌПЩвдДгЗДгІЛьКЯЮяжаРыЮіГіРДЁЃДЫРрИДКЯЮяЕФаЮГЩЃЌвдМАЫќУЧЕФЮШЖЈадКЭЫќУЧзЊБфЮЊЫЋИКРызгЕФПЩФмадЃЌЖМЮЊSNAr2РњГЬЬсЙЉСЫНсТладЕФжЄОнЁЃ
3.1.3 БНШВРњГЬ
ФГаЉЗМЯузхЧзКЫШЁДњЗДгІЕФЬиЕуЯдШЛЪЧКЭАДSNAr1РњГЬКЭSNAr2РњГЬНјааЕФЗДгІВЛвЛбљЁЃетаЉЗДгІЗЂЩњдкУЛгаЛюЛЏЛљЭХЕФЗМЯуТБЛЏЮяЩЯЃЌашвЊБШНЯЧПЕФМюРДДпЛЏЃЌЖјЧвНјШыЛљЭХВЛЪЧгРдЖЕФШЁДњАЂРыШЅЛљЭХЫљдкЕФЮЛжУЩЯЁЃР§ШчЃЌ1Ѓ14CТШБНКЭАБЛЏМизїгУаЮГЩСНжжВЛЭЌЕФВњЦЗЃК
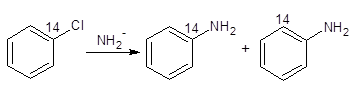
етРяаЮГЩЕФСНжжВњЦЗЕФСПМИКѕЪЧЯрЕШЕФЁЃ
етжжЗДгІЪЧЭЈЙ§ЯћГ§ЃМгГЩРњГЬНјааЕФЁЃЯТУцЪЧжЇГжетвЛЛњРэЕФвЛаЉжЄОнЃК
ЃЈ1ЃЉШєЗМЛљТБАќРЈСНИіСкЮЛШЁДњЛљЃЌетИіЗДгІОЭВЛФмЗЂЩњЃЛ
ЃЈ2ЃЉБфЮЛЃЈcineЃЉШЁДњЃЛ
ЃЈ3ЃЉТБЛЏЮяЕФЗДгІадЫГађЪЧЃКBr>I>Cl>>FЃЈЗДгІдквКNH3жагыKNH2НјааЪБЃЉЕФЪТЪЕЃЌЫЕУїSNArЛњРэдкДЫДІЪЧВЛЦ№зїгУЕФЁЃ




